金沙集团3354.c.cav的产品展示navigation

电话:021-35183767
021-35183767
传真:021-35183767-8008
qq:2881513768
地址:上海市闵行区兴梅路485号 xingmei rd 485shanghaichina
ugo basile抓力测量仪
时间:2023-12-21来源:本站作者:玉研仪器

详细介绍
基于大小鼠抵制向后运动本能自动测量其前肢、后肢、或四肢抓力大小,用于评估物质(药物、毒素、肌肉松弛剂)和条件(疾病、衰老、神经损伤)对肌肉力量的影响。
动物疼痛研究中常采用机械刺痛的形式评估异常性疼痛及痛觉过敏,运动协调测试常采用rota-rod转棒仪,神经毒性及退行性疾病常采用行为学测试方案,但上述评估方式都缺乏对动物肌肉力量进行评估,抓力测量仪以肌肉损伤和力量改变为切入点可弥补多类研究中关于肌肉测试的空白。
ugo basile抓力测量仪是一款评估大、小鼠前后肢及四肢抓力的经典设备。可测试肌肉松驰剂、神经抑制剂、兴奋剂等对肢体力量的影响,同时也可对动物的衰老、神经损伤、骨骼肌肉损伤、术后恢复程度进行鉴定,适用范围广泛。ugo basile抓力测量仪操作简单,使用方便,指标明确,特异性强而广泛地被国内外科研工作者使用,并收到了很好的实验效果。
设备由控制器、各类抓杆、力传感器、脚踏开关构成。选取合适的抓杆安置在力传感器凹槽中,使大小鼠爪子握住抓杆,动物呈水平体位。当水平反向拉动动物尾巴时,啮齿动物本能地会抓住抓杆,试图阻止这种不自主的向后运动,直到施加的拉力超过它们的抓力。当大小鼠失去对抓杆的抓握后,控制器自动存储峰值抓力并实时显示。

优势特点:
一、标配多种测试抓杆,可进行全面抓力测试
ugo basile抓力测量仪标配多种类型抓力测试杆,可针对不同动物模型,测量大小鼠前肢、后肢、四肢分别的抓力大小,应用范围广,为同类型产品中之最。标配抓杆有:金属t杆、三角型抓杆、可倾斜条形抓杆、网格抓杆、半网格抓杆。
二、系统自动校准、自动清零
ugo basile抓力测量仪采用专用存储芯片记录所有校准参数,无需进一步校准;此外,控制器会在每次测量时提示自动归零程序,以自动调整任何基线偏移。
三、自动记录抓力峰值,采样频率高
相较于同类产品,ugo basile 抓力测量仪的传感器有着极高的采样频率,这使得控制器能够在连续变力上精细地截取峰值。当鼠爪放弃对抓杆抓握时,控制器实时记录峰值大小和测试时间,如有特殊应用时,也可运用脚踏开关进行手动记录峰值大小。
四、三种量程任意切换,存储容量大
设备具有三种量程:0-100g、0-500g、1500g,精度为0.1g,量程可在控制器任意切换以适用多种不同情况应用。控制器可存储数百个测试结果。
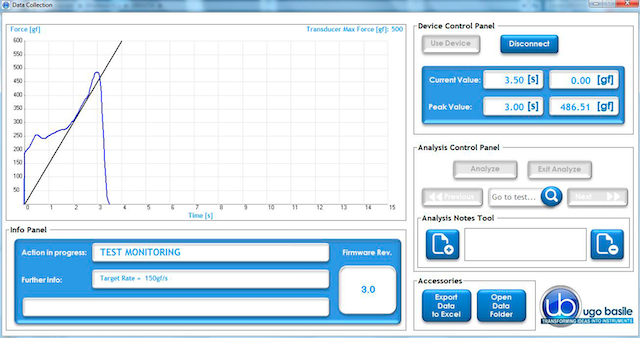
五、可设定拉力斜率,抓力曲线直观可视
ugo basile 抓力测量仪具有自定义线性增力范围设置,可根据不同模型设置相应的拉力斜率,最大限度提升线性增力的稳定情况。实验人员施加拉力时尝试匹配设定线性增力的直线,可提高实验结果准确度与一致性。


抓力测量仪可评估大小鼠前后肢及四肢抓力大小,主要为评估动物肌肉功能和神经系统状况,可应用于衰老表型分析、神经肌肉退行性变化、肌肉萎缩症、骨骼相关疾病、运动控制障碍、帕金森病、亨廷顿病等疾病研究。
| 47200 | 抓力测量仪完整套装,包含控制器、力传感器、黑色基座、软件及6款抓杆 |


参考文献:
1.ahmed s, kwatra m, ranjan panda s, et al. andrographolide suppresses nlrp3 inflammasome activation in microglia through induction of parkin-mediated mitophagy in in-vitro and in-vivo models of parkinson disease. brain behav immun. 2021;91:142-158. doi:10.1016/j.bbi.2020.09.017
2.yan d, yao j, liu y, et al. tau hyperphosphorylation and p-creb reduction are involved in acrylamide-induced spatial memory impairment: suppression by curcumin. brain behav immun. 2018;71:66-80. doi:10.1016/j.bbi.2018.04.014
3.gautam m, jara jh, kocak n, et al. mitochondria, er, and nuclear membrane defects reveal early mechanisms for upper motor neuron vulnerability with respect to tdp-43 pathology. acta neuropathol. 2019;137(1):47-69. doi:10.1007/s00401-018-1934-8
4.wertz mh, pineda ss, lee h, et al. interleukin-6 deficiency exacerbates huntington's disease model phenotypes. mol neurodegener. 2020;15(1):29. doi:10.1186/s13024-020-00379-3
5.el-sitt s, soueid j, maalouf k, et al. exogenous galactosylceramide as potential treatment for cln3 disease. ann neurol. 2019;86(5):729-742. doi:10.1002/ana.25573
6.batallé g, bai x, pouso-vázquez e, et al. the recovery of cognitive and affective deficiencies linked with chronic osteoarthritis pain and implicated pathways by slow-releasing hydrogen sulfide treatment. antioxidants (basel). 2021;10(10):1632. doi:10.3390/antiox10101632
7.wijaya yt, setiawan t, sari in, et al. ginsenoside rd ameliorates muscle wasting by suppressing the signal transducer and activator of transcription 3 pathway. j cachexia sarcopenia muscle. 2022;13(6):3149-3162. doi:10.1002/jcsm.13084
8.goebel a, krock e, gentry c, et al. passive transfer of fibromyalgia symptoms from patients to mice. j clin invest. 2021;131(13):e144201. doi:10.1172/jci144201
9.zhang w, zhou m, lu w, et al. cntnap4 deficiency in dopaminergic neurons initiates parkinsonian phenotypes. theranostics. 2020;10(7):3000-3021. doi:10.7150/thno.40798
10.cocozza g, di castro ma, carbonari l, et al. ca2 -activated k channels modulate microglia affecting motor neuron survival in hsod1g93a mice. brain behav immun. 2018;73:584-595. doi:10.1016/j.bbi.2018.07.002
您想了解更多详细资料吗?
请与我们联系:
tel:021-35183767,021-54377179
18502129044
qq:3007536621
微信:yuyanbio
mail:yuyanbio@126.com
欢迎您的咨询!
